
Cara Menghitung Ph Asam Lemah Satu Manfaat
Dapatkan pelajaran, soal. dan rumus larutan asam basa lengkap SMA.. Reaksi Asam Basa & pH. Setelah memahami konsepnya, kini kamu bisa mencoba untuk mempelajari materi yang lebih dalam, yaitu materi reaksi asam basa & pH. Reaksi asam basa sendiri didefinisikan sebagai reaksi antara asam dan basa yang nantinya akan menghasilkan air dan garam.

Cara Menghitung pH Larutan Asam, Basa, Garam Beserta Contoh Soal dan Pembahasan Asymmetrical Life
Hubungan antara pH dan pOH adalah : pH + pOH = pKw. dimana Kw adalah konstanta disosiasi air (menghasilkan H + dan OH −) yang bernilai 10 − 14, sehingga persamaan di atas menjadi. pH + pOH = 14. Suatu larutan akan bersifat asam bila jumlah H + lebih besar dari jumlah OH −, sehingga pada kondisi netral, pH = pOH = 7.

pH Campuran Basa lemah dan Basa Kuat Kimia SMA YouTube
PH larutan dapat dihitung menggunakan rumus pH = -log [H+], sehingga pH larutan = -log (1 x 10^-11) = 11. Demikianlah penjelasan mengenai rumus asam basa dan hal yang bersangkut paut dengannya. Materi ini menjadi pokok pembahasan pada kurikulum pendidikan nasional yang akan dipelajari oleh siswa- siswi SMP kelas 9 pada mata pelajaran Kimia .

PERHITUNGAN pH ASAM LEMAH DAN BASA LEMAH YouTube
Halo semuanya. Jumpa lagi di channel @5NChemistry, kali ini menjelaskan kepada kalian tentang bagaimana cara menghitung pH suatu larutan asam dan basa. Mater.

SOALSOAL Mencari Massa AsamBasa apabila yang diketahui pH dan Volume Larutannya Q&A YouTube
Di mana jika suatu larutan mempunyai pH<7, maka larutan tersebut bersifat asam, pH>7 bersifat basa, dan pH=7 bersifat netral.. Konsentrasi ion OH- dihitung dengan rumus asam-basa sederhana seperti berikut. [OH-] = n × Mb. Keterangan: n= Banyaknya ion OH-Ma = Molaritas basa. 2. Zat dalam larutan terdiri atas asam kuat dan basa lemah dengan.

Larutan Asam dan Basa RUMUS LENGKAP KELAS 11 DAN CONTOHNYA Derajat Keasaman pH Indikator
Ketahuilah arti pH. pH adalah konsentrasi ion hidrogen dalam suatu larutan. Larutan dengan konsentrasi ion hidrogen yang tinggi bersifat asam. Larutan dengan konsentrasi ion hidrogen yang rendah bersifat basa, atau juga dikenal sebagai alkali. Ion-ion hidrogen, juga dikenal sebagai hidronium, dituliskan secara singkat menjadi H+ atau H3O+.

Cara Menghitung pH dan pOH asam Lemah dan Basa Lemah YouTube
Tingkat keasaman/pH larutan asam basa tergantung pada molaritas ion H+ dalam larutan. Jika molaritas ion H+ semakin besar, maka semakin asam larutan itu. 1. Rumus pH Nilai pH larutan asam basa diperoleh sebagai hasil negatif logaritma 10 dari molaritas ion H+. Secara matematis dapat dituliskan: pH = -log [H+] Keterangan: pH = derajat keasaman [H+]

Super Mudah Perhitungan pH Asam Basa (Part 1) YouTube
Sementara itu, asam kuat + basa kuat = netral. Artinya apabila reaksi asam kuat dicampurkan dengan basa kuat akan menghasilkan larutan dengan pH 7 atau netral.. Rumus asam basa. Rumus asam basa di bawah ini akan berguna saat pembuatan laporan praktikum titrasi asam basa. Sedikit informasi, titrasi asam basa adalah prosedur untuk menentukan.

Cara Menghitung pH Garam dari Asam Kuat dan Basa Lemah Materi hidrolisis garam Kimia SMA Kelas
Kalau pada suhu 25℃, pH < 7 bersifat asam, pH = 7 bersifat netral, dan pH > 7 bersifat basa. Derajat keasaman dan kebasaan suatu larutan. (dok. Flickr/boellstiftung) Semakin kecil nilainya, maka larutan tersebut akan semakin asam. Misalnya antara larutan dengan pH 3 dan 1, akan lebih kuat konsentrasi asam dengan pH 1 daripada 3.

Mengenal Rumus Ph Beserta Contoh Soal Dan Cara Menghitungnya Kumparan Riset
Rumus untuk menghitung nilai pH dari sebuah konsentrasi ion hidronium. Perbedaan kuantitatif antara zat asam dan alkali dapat ditentukan dengan melakukan pengukuran nilai pH. Beberapa contoh nilai pH zat dan bahan kimia yang kita gunakan setiap hari diberikan dalam gambar 4:. Bukan hanya asam dan basa yang menunjukkan perilaku disosiasi.

MENGHITUNG pH BASA KUAT DAN BASA LEMAH YouTube
Valensi basa adalah jumlah ion OH − yang dihasilkan per unit rumus basa. basa lemah (contoh: NH 3, CH 3 NH 2, C 6 H 5 NH 2). Contoh Soal Larutan Asam Basa dan Pembahasan. Tentukan pH masing-masing larutan berikut. a. HCl 0,007 M b. HCOOH 0,05 M (K a = 1,8 × 10 −4) c. Ca(OH) 2 0,001 M d.
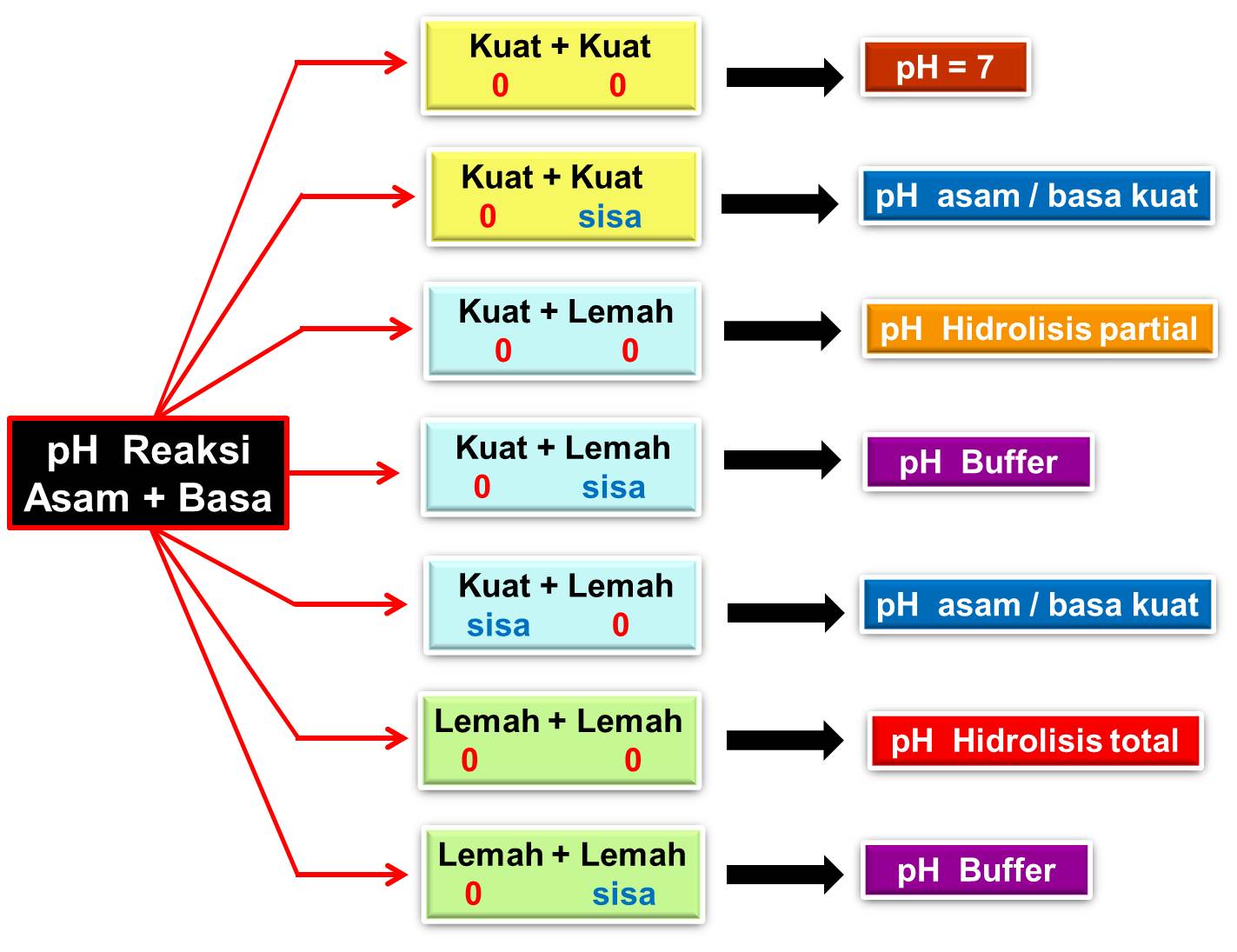
CINTA KIMIA PH REAKSI ASAM DAN BASA
Perhitungan pH basa lemah. Sama halnya dengan asam lemah, untuk menghitung pH basa lemah nilai [OH -] dan tetapan Kb harus sudah diketahui terlebih dahulu. Selanjutnya, kamu bisa mulai menghitung pH basa lemah melalui rumus berikut ini:

Perhitungan pH Asam Basa Kuat, Lemah, dan Poliprotik Kimia Kelas XI YouTube
Reaksi Asam Basa - Rumus Kimia - Contoh Soal dan Jawaban. Ilustrasi dans sumber foto: Pixabay Dapat dikatakan bahwa molekul air adalah asam konjugat ion hidroksida setelah hidroksida mendapat proton hidrogen yang diberikan oleh amonium.Di sisi lain, amonia adalah basa konjugat untuk amonium asam setelah amonium telah menyerahkan ion hidrogen untuk menghasilkan molekul air.

contoh soal menghitung ph asam kuat dan basa kuat Menghitung soal
Jadi, pH larutan asam etanoat tersebut adalah 2,72. 3. Larutan Basa Kuat. Cara menghitung pH larutan basa kuat hampir mirip dengan menghitung asam kuat. Rumus yang bisa digunakan adalah -log dikali . adalah dari konsentrasi ion dalam larutan, b adalah jumlah ion yang dilepaskan., dan M adalah konsentrasi larutan basa. Simak contoh soal berikut ini.

Lagu kimia rumus dan langkah menghitung pH larutan asam basa YouTube
Modul, Rumus, & Soal Asam & Basa. Kalau kebetulan kamu ingin belajar lebih tentang asam & basa dalam ilmu kimia, kamu bisa menyimak pembahasannya berikut. Setelahnya, kamu bisa mengerjakan kuis berupa latihan soal untuk mengasah kemampuan belajarmu. Seringkali kita mendengar istilah asam dan basa. Istilah asam biasnya untuk mendefinisikan rasa.

Contoh Soal pH dan pOH Asam Kuat dan Basa Kuat YouTube
Pada gambar di sebelah kanan, satu molekul H2O bertindak sebagai basa dan mendapatkan H + menjadi H3O+ sementara lainnya bertindak selaku asam dan kehilangan H+ dan menjadi OH −. Contoh lain dapat dilihat pada aluminium hidroksida Al (OH)3. Asam Basa pH - Rumus Kimia - Penjelasan, Contoh Soal dan Jawaban.